بازده واکنش های شیمیایی
چکیده: در ادامه مبحث واکنش های شیمیایی و استوکیومتری به مسائل مربوط به بازده واکنش های شیمیایی و مقایسه مقدار فراورده مورد انتظار از محاسبه های استوکیومتری با مقدار فراورده ای که در عمل تولید می شود، خواهیم پرداخت.
شرح درس:
در بسیاری از واکنش های شیمیایی که برای تهیه مواد شیمیایی به کار می روند، مقدار فراورده های به دست آمده کمتر از مقدار محاسبه شده است و مسایل مربوط به بازده واکنش های شیمیایی مطرح می شود.
بازده نظری: جرم فراورده مورد نظر است که با توجه به محاسبه های استوکیومتری انتظار داریم به دست آید.
بازده عملی: جرم فراورده مورد نظر است که در عمل به دست می آید.
در اغلب موارد بازده عملی کمتر از بازده نظری است. این امر می تواند به دلیل ناخالصی واکنش دهنده ها، انجام واکنش های جنبی و پیش بینی نشده و هم چنین عدم امکان جمع آوری کامل فراورده ها باشد. در عمل مقداری از واکنش دهنده ها و یا فراورده ها به طرق مختلف هدر می روند.
بازده درصدی: بازده درصدی یک واکنش نسبت دو بازده عملی و نظری به یکدیگر است و به صورت زیر تعریف می شود:
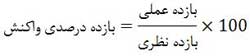
اغلب واکنش ها بازده ای کمتر از صد در صد دارند اما شیمی دان ها همواره در جهت افزایش بازده درصدی فرایندهای صنعتی و آزمایشگاهی تلاش می کنند.
روش به دست آوردن بازده درصدی واکنش:
روش اول
گام نخست: پیدا کردن واکنش دهنده محدود کننده
گام دوم: محاسبه بازده نظری واکنش از روی مقدار واکنش دهنده محدود کننده
گام سوم: محاسبه بازده درصدی واکنش
روش دوم- روش تناسب
برای به دست آوردن بازده درصدی واکنش می توان از روش های زیر استفاده کرد:
در این روش مقدار واکنش دهنده مورد نظر را در R/100 ضرب می کنیم. R/100 همان بازده درصدی است که هرچه مقدار آن کوچک تر باشد بدین معنی است که مقدار کمتری از واکنش دهنده ها به دلایل مختلف، تبدیل به فراورده های قابل دسترس شده اند و بدین ترتیب فراورده کمتری به دست می آید.
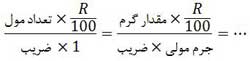
مثال: چند گرم پتاسیم کلرات ٨٠ درصد خالص اگر بر اثر گرما به میزان 50 درصد تجزیه شود، 6.72 لیتر گاز اکسیژن در شرایط STP آزاد می شود؟ (O=16,Cl=35.5 , K=39)